CXCR2抑制可增强非酒精性脂肪性肝炎和肝细胞癌的免疫治疗
发布日期:2023-08-16 浏览次数:1640
前言:
题目:CXCR2 inhibition enables NASH-HCC immunotherapy
发表时间:2022 年 4 月 27 日
期刊:GUT
影响因子:23.06

背景:
原发性肝癌是全球最常见和最致命的恶性肿瘤之一。肝细胞癌(HCC)占原发性肝癌的85%,现在大部分 HCC 归因于非酒精性脂肪性肝炎 (NASH)。
免疫检查点抑制 (ICI) 已成为 HCC 的一种治疗方式,然而,只有少数(高达 30%)的 HCC 患者对免疫治疗有反应。由于 NASH 诱导的肝脏免疫成分改变,特别是耗尽的 CD8+PD1+T 细胞数量增加,导致 NASH 背景下的 HCC 对免疫治疗的反应较低。因此,HCC 的先进治疗策略将需要更深入地了解肿瘤微环境的复杂免疫景观。
已有研究表明具有较低侵袭性癌症和持续肝损伤(纤维化)区域富含 CD8+T 细胞、B 细胞和 CD11b+CD15 + 中性粒细胞。越来越多的证据表明中性粒细胞在多种癌症中具有促肿瘤或抗肿瘤功能,肿瘤微环境中中性粒细胞生物学的调节是否会影响 NASH-HCC 对抗 PD1 免疫疗法的耐药性及机制目前不够了解。
该研究结果表明, CXCR2 的拮抗作用与抗 PD1联合疗法重新编程了肿瘤中性粒细胞的表型,增强了它们与 CD8+T 细胞和常规树突状细胞 (cDC) 的关联。重塑肿瘤免疫微环境与依赖 T 细胞和 DC细胞的肿瘤负荷减少和存活率增加有,该研究结果为中性粒细胞表型修饰联合 ICI 改善 NASH-HCC 的治疗提供科学依据。
研究思路
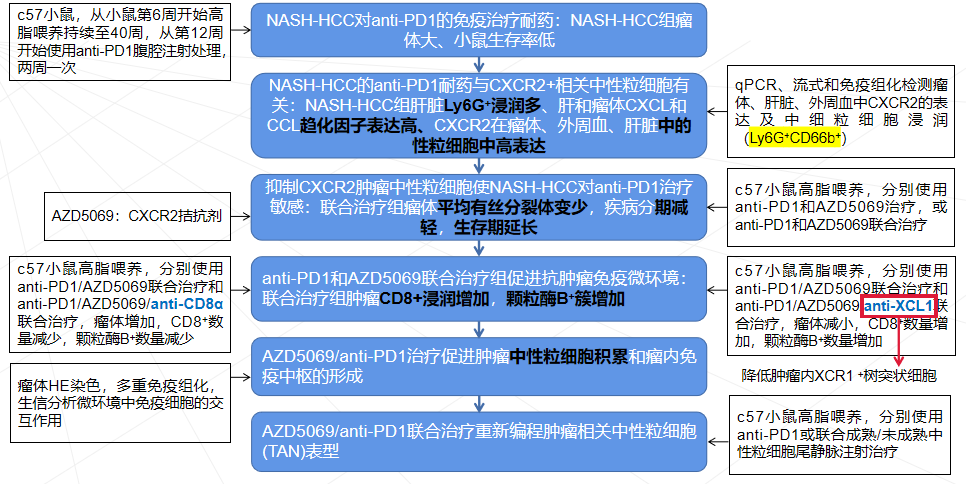
创新之处
主要试剂及检测指标:
1. CXCR2拮抗剂:AZD5069,100 mg/kg,灌胃
2. anti-PD1:Biolegend,200 ug,腹腔注射
3. anti-CD8α:Biolegend,50 ug,腹腔注射
4. anti-XCL1:R&D systems MAB486,,腹腔注射
5. 中性粒细胞表面标志蛋白:Ly6G+CD66b+
抗 PD1 和 CXCR2 抑制剂结合选择性地将肿瘤相关中性粒细胞 (TAN) 重编程为抗肿瘤表型。未来,可以选择性地操纵肿瘤相关中性粒细胞以采用抗肿瘤表型,从而释放其在癌症治疗中的潜力。CXCR2 拮抗剂与 ICI 治疗相结合以增强 NASH-HCC(以及可能在其他病因的HCC中)的治疗益处的能力也值得临床研究。
前言:
题目:CXCR2 inhibition enables NASH-HCC immunotherapy
发表时间:2022 年 4 月 27 日
期刊:GUT
影响因子:23.06

背景:
原发性肝癌是全球最常见和最致命的恶性肿瘤之一。肝细胞癌(HCC)占原发性肝癌的85%,现在大部分 HCC 归因于非酒精性脂肪性肝炎 (NASH)。
免疫检查点抑制 (ICI) 已成为 HCC 的一种治疗方式,然而,只有少数(高达 30%)的 HCC 患者对免疫治疗有反应。由于 NASH 诱导的肝脏免疫成分改变,特别是耗尽的 CD8+PD1+T 细胞数量增加,导致 NASH 背景下的 HCC 对免疫治疗的反应较低。因此,HCC 的先进治疗策略将需要更深入地了解肿瘤微环境的复杂免疫景观。
已有研究表明具有较低侵袭性癌症和持续肝损伤(纤维化)区域富含 CD8+T 细胞、B 细胞和 CD11b+CD15 + 中性粒细胞。越来越多的证据表明中性粒细胞在多种癌症中具有促肿瘤或抗肿瘤功能,肿瘤微环境中中性粒细胞生物学的调节是否会影响 NASH-HCC 对抗 PD1 免疫疗法的耐药性及机制目前不够了解。
该研究结果表明, CXCR2 的拮抗作用与抗 PD1联合疗法重新编程了肿瘤中性粒细胞的表型,增强了它们与 CD8+T 细胞和常规树突状细胞 (cDC) 的关联。重塑肿瘤免疫微环境与依赖 T 细胞和 DC细胞的肿瘤负荷减少和存活率增加有,该研究结果为中性粒细胞表型修饰联合 ICI 改善 NASH-HCC 的治疗提供科学依据。
研究思路

创新之处
主要试剂及检测指标:
1. CXCR2拮抗剂:AZD5069,100 mg/kg,灌胃
2. anti-PD1:Biolegend,200 ug,腹腔注射
3. anti-CD8α:Biolegend,50 ug,腹腔注射
4. anti-XCL1:R&D systems MAB486,,腹腔注射
5. 中性粒细胞表面标志蛋白:Ly6G+CD66b+
抗 PD1 和 CXCR2 抑制剂结合选择性地将肿瘤相关中性粒细胞 (TAN) 重编程为抗肿瘤表型。未来,可以选择性地操纵肿瘤相关中性粒细胞以采用抗肿瘤表型,从而释放其在癌症治疗中的潜力。CXCR2 拮抗剂与 ICI 治疗相结合以增强 NASH-HCC(以及可能在其他病因的HCC中)的治疗益处的能力也值得临床研究。



